Associação Portuguesa de Investigação em Cancro
Descobertos novos péptidos para terapia dirigida de cancro de mama
Descobertos novos péptidos para terapia dirigida de cancro de mama
Quais são as principais limitações contemporâneas na deteção precoce de cancro de mama?
Qual o subtipo celular com prognóstico mais reservado?
Qual a importância de novos alvos celulares na terapia dirigida?
O cancro da mama triplo negativo é um subtipo celular altamente maligno, caracterizado pela inexistência de biomarcadores conhecidos. Desta forma, o prognóstico reservado deve-se à sua incapacidade de responder a terapias clássicas hormonais, tornando-se altamente metastático. Este tipo de cancro da mama tem ganho forte interesse nos últimos anos, pela necessidade de identificar novos alvos terapêuticos que poderão ser usados, quer em diagnóstico precoce, quer no desenvolvimento de terapêuticas dirigidas. Devido à sua elevada heterogeneidade tumoral, torna-se fundamental identificar e isolar biomarcadores específicos de subtipos celulares e promover a terapia individualizada.
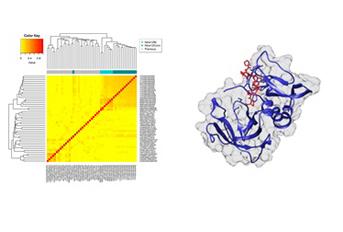
Na Universidade do Minho, um estudo focou-se na exploração de metodologias de base genética em fagos – “phage display” –, que permitiu a identificação e isolamento de novos péptidos específicos usando a linha celular MDA-MB-231, representativa de cancro da mama triplo negativo. A metodologia usada aliada a uma rigorosa análise bioinformática permitiu a identificação e caracterização de dois novos péptidos (PRWAVSP e DTFNSFGRVRIE), que ostentaram uma forte interação com a linha celular de interesse. Observou-se, também, uma elevada especificidade destes novos péptidos, validada pela sua fraca adesão à linha celular controlo MDA-MB-435. Com estes resultados, foi possível concluir que o “phage display” é uma técnica promissora na identificação de novos alvos terapêuticos e no isolamento de péptidos capazes de aderir às células cancerígenas. No futuro, estes péptidos poderão apresentar uma valiosa aplicabilidade na clínica oncológica, contribuindo para o desenvolvimento de terapias mais específicas e dirigidas para cancro da mama triplo negativo.
Autores e Afiliações:
Franklin L. Nobrega, Débora Ferreira, Ivone M. Martins, Maria Suarez-Diez, Joana Azeredo, Leon D. Kluskens and Lígia R. Rodrigues
Centre of Biological Engineering (CEB), University of Minho
Laboratory of Systems and Synthetic Biology, Wageningen University and Research Centre
Abstract:
Background: Claudin-low breast carcinoma represents 19% of all breast cancer cases and is characterized by an aggressive progression with metastatic nature and high rates of relapse. Due to a lack of known specific molecular biomarkers for this breast cancer subtype, there are no targeted therapies available, which results in the worst prognosis of all breast cancer subtypes. Hence, the identification of novel biomarkers for this type of breast cancer is highly relevant for an early diagnosis. Additionally, claudin-low breast carcinoma peptide ligands can be used to design powerful drug delivery systems that specifically target this type of breast cancer.
Methods: In this work, we propose the identification of peptides for the specific recognition of MDA-MB-231, a cell line representative of claudin-low breast cancers, using phage display (both conventional panning and BRASIL). Binding assays, such as phage forming units and ELISA, were performed to select the most interesting peptides (i.e., specific to the target cells) and bioinformatics approaches were applied to putatively identify the biomarkers to which these peptides bind.
Results: Two peptides were selected using this methodology specifically targeting MDA-MB-231 cells, as demonstrated by a 4 to 9 log higher affinity as compared to control cells. The use of bioinformatics approaches provided relevant insights into possible cell surface targets for each peptide identified.
Conclusions: The peptides herein identified may contribute to an earlier detection of claudin-low breast carcinomas and possibly to develop more individualized therapies.
Revista: BMC Cancer
Link: https://bmccancer.biomedcentral.com/articles/10.1186/s12885-016-2937-2






